콘텐츠
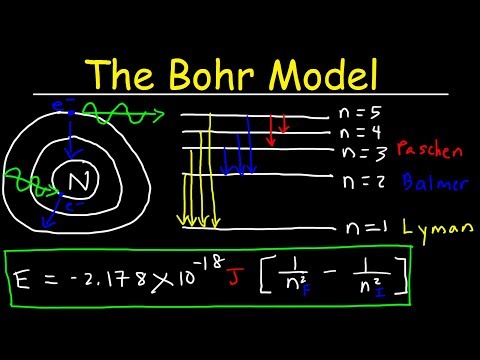
수소 원자의 발머 계열은 가능한 전자 전이와 엔 과학자들이 관찰하는 방출 파장의 2 위치. 양자 물리학에서 전자가 원자 주위의 다른 에너지 수준 사이에서 전이 할 때 (주 양자 수로 설명 됨) 엔) 광자를 방출하거나 흡수합니다. Balmer 시리즈는 더 높은 에너지 레벨에서 두 번째 에너지 레벨로의 전환 및 방출 된 광자의 파장을 설명합니다. Rydberg 공식을 사용하여이를 계산할 수 있습니다.
TL; DR (너무 길고 읽지 않음)
다음을 기준으로 수소 발머 계열 전이의 파장을 계산하십시오.
1/λ = 아르 자형H ((1/22) − (1 / 엔22))
어디 λ 파장입니다 아르 자형H = 1.0968 × 107 엠−1 과 엔2 전자가 전이하는 상태의 주요 양자 수입니다.
Rydberg 공식 및 Balmer의 공식
Rydberg 공식은 관측 된 방출의 파장을 전이와 관련된 주요 양자 수와 관련시킵니다.
1/λ = 아르 자형H ((1/엔12) − (1 / 엔22))
그만큼 λ 기호는 파장을 나타내고 아르 자형H 수소에 대한 Rydberg 상수이며 아르 자형H = 1.0968 × 107 엠−1. 이 공식은 두 번째 에너지 레벨과 관련된 전환뿐만 아니라 모든 전환에 사용할 수 있습니다.
발머 시리즈 엔1 = 2, 주요 양자 수 값 (엔)는 전환이 고려되는 두 가지입니다. Balmer의 공식은 다음과 같이 쓸 수 있습니다 :
1/λ = 아르 자형H ((1/22) − (1 / 엔22))
발머 시리즈 파장 계산
계산의 첫 단계는 고려중인 전환의 기본 양자 번호를 찾는 것입니다. 이는 단순히 "에너지 수준"에 수치를 두는 것을 의미합니다. 세 번째 에너지 수준은 엔 = 3, 네 번째는 엔 = 4 등. 이들은 그 자리에 간다 엔2 위의 방정식에서.
방정식의 일부를 괄호로 계산하여 시작하십시오.
(1/22) − (1 / 엔22)
필요한 것은 엔2 이전 섹션에서 찾았습니다. 에 대한 엔2 = 4, 당신은 얻을 :
(1/22) − (1 / 엔22) = (1/22) − (1 / 42)
= (1/4) − (1/16)
= 3/16
이전 섹션의 결과에 Rydberg 상수를 곱하고 아르 자형H = 1.0968 × 107 엠−1, 1 /에 대한 값을 찾으려면λ. 공식과 예제 계산은 다음을 제공합니다.
1/λ = 아르 자형H ((1/22) − (1 / 엔22))
= 1.0968 × 107 엠−1 × 3/16
= 2,056,500 미터−1
1을 이전 섹션의 결과로 나누어 전이의 파장을 찾으십시오. Rydberg 공식은 역수 파장을 제공하므로 파장의 결과를 역수로 구해야합니다.
따라서 예제를 계속 진행하십시오.
λ = 1 / 12,056,500m−1
= 4.86 × 10−7 엠
= 486 나노 미터
이것은 실험을 기반으로이 전이에서 방출 된 확립 된 파장과 일치합니다.