콘텐츠
과학자들은 화학 반응이있는 용액 내에서 물질의 양을 찾기 위해 직접적인 적정에 의존합니다. 올바르게 수행하면이 과정에서 특수 산과 실험실 유리를 사용하여 화학 물질의 양을 매우 정확하게 묘사 할 수 있습니다. 적정이 제대로 작동하려면 과학자가 분석 할 수 있도록 마지막 복합물이 신속하게 형성되어야합니다.
정의
직접 적정은 물질의 함량을 정량적으로 결정하는 방법입니다. 과학자들은 반응물에 대해서는 알고 있지만 반응물의 양은 모릅니다. 직접 적정은 때때로 분석 물이라고하는 분석 된 물질에 반응하는 지표를 기반으로합니다. 다른 경우에, 상기 방법은 특정 유형의 금속의 개별 원자 또는 분자 인 첨가 된 금속 이온의 사용에 기초한다.
에틸렌 디아민 테트라 아세트산 및 전위차 법
기술자는 금속 이온 표시기가있는 에틸렌 디아민 테트라 아세트산을 사용하여 적정을 수행 할 수 있습니다. 이 방법은 반응이 너무 느려 적정이 비현실적이기 때문에 모든 상황에서 작동하지는 않습니다. 사용 된 금속 이온은 분석 물보다 안정성이 낮아야합니다. 직접 적정의 또 다른 방법은 특정 가용 전극을 가진 금속 이온으로 종말점 검출에 사용되는 전위차 법입니다. 종말점은 적정 프로세스가 끝나는 지점입니다.
복합 계 적정
복잡한 적정을 위해 과학자들은 아미노 폴리 카르 복실 산을 사용하여 금속을 식별합니다. 유색 착물이 형성되고 과학자들은이 형성으로부터 수집 된 데이터를 사용하여 분석 물의 양을 결정합니다. 착물 적정법의 직접적인 방법은 착물 화합물 용액으로 적정 된 금속-염 용액의 사용을 포함한다. 착화 화합물 용액은 다른 원자 또는 화합물과 착물을 형성하는 원자 또는 화합물을 함유한다. 과학자들은 추가 지표에서 등가 점을 찾습니다. 등가 점은 첨가 된 적정 제가 화학량 론적으로 분석 물과 동일 할 때입니다. 화학 양론은 화학 반응 균형을 포함합니다.
뷰렛 솔루션
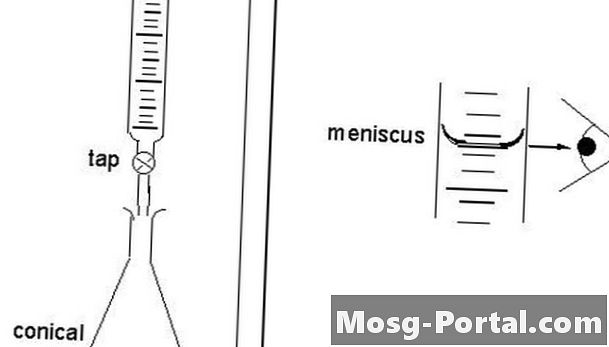
과학자가 종말점에 직접 접근하기 때문에 직접 적정을 "직접"이라고합니다. 적정 제는 뷰렛에서 방울을 통해 용액에 들어가므로 최종 방울이 끝점을 초과하지 않습니다. 직접 적정을 통해 과학자들은 용액에 포함 된 용해성 물질을 처리합니다.이 물질은 적 정액이라는 용기에 들어 있습니다. 표준화 된 솔루션을 적정 제라고합니다. 종점은 지표의 도움으로 도구 또는 시각적으로 결정됩니다. 과학자들은 적정량의 소량의 액체를 방출하는 정밀 탭이있는 수직 및 원통형 유리 제품인 올바른 뷰렛에 적정 제를 첨가합니다. 과학자들은 뷰렛을 30 ~ 100 % 용량으로 채 웁니다.